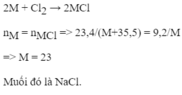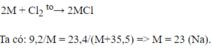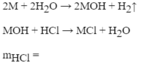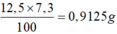Đốt cháy hoàn toàn 11,7 gam một kim loại hóa trị I trong bình đựng khí clo thu được 22,35 gam muối. Xác định tên kim loại. Cho biết Na = 23; K = 39; Ag = 108; Cl = 35,5.

Những câu hỏi liên quan
Cho luống khí clo dư tác dụng với 9,2 gam kim loại sinh ra 23,4g muối kim loại hóa trị I. Xác định công thức hóa học của muối đó (Na=23, Ag=108, Li=7, K=39, Cl=35,5).
Cho luồng khí clo (dư) tác dụng với 9,2g kim loại hóa trị I, tạo ra 23,4 g muối. Xác định tên kim loại (Na=23, Ag=108, Li=7, K=39, Cl=35,5).
Hòa tan hoàn toàn 0,575 gam một kim loại kiềm vào nước. Để trung hòa dung dịch thu được cần dùng 12,5 gam dung dịch HCl 7,3% (Li=7, Na=23, K=39, Rb=85, H=1, Cl=35,5). Xác định tên kim loại kiềm.
Đốt cháy hoàn toàn 4,6 gam một kim loại kiềm X trong khí clo dư, thu được 11,7 gam muối. Kim loại kiềm X là:
A.Na B.Li C.K D.Cs
Gọi nguyên tử khối của kim loại A là A.
Phương trình hóa học của phản ứng:
2A + Cl2 → 2ACl
mA = 4,6g, mACl = 11,7g.
Có nA = nACl
nA = 4.6/A, nACl = 11.7 /(A + 35,5)
=> 4,6 x (A + 35,5) = A x 11.7
=> A = 23. Vậy kim loại A là Na.
Đúng 0
Bình luận (0)
Cho 9,6 gam một kim loại R hóa trị 2 tan hoàn toàn trong dung dịch HNO3
loãng thu được 2,24 lít khí NO duy nhất (điều kiện tiêu chuẩn).
a. Xác định tên của R?
b. Xác định khối lượng muối thu được?
(Cho khối lượng nguyên tử: K = 39; Ag = 108; Fe = 56; Cu = 64; Al = 27;
Pb = 207; H = 1; N = 14; O = 16).
nNO = 2,24/22,4 = 0,1 (mol)
PTHH: 3R + 8HNO3 (loãng) -> 3R(NO3)2 + 2NO + 4H2O
nR(NO3)2 = nR = 3/2 . 0,1 = 0,15 (mol)
M(R) = 9,6/0,15 = 64 (g/mol)
=> R là Cu
mCu(NO3)2 = 0,15 . 188 = 28,2 (g)
Đúng 2
Bình luận (0)
Cho 2,7 gam một kim loại R hóa trị 3 tan hoàn toàn trong dung dịch HNO3
loãng thu được 2,24 lít khí NO duy nhất (điều kiện tiêu chuẩn).
a. Xác định tên của R?
b. Xác định khối lượng muối thu được?
(Cho khối lượng nguyên tử: K = 39; Ag = 108; Fe = 56; Cu = 64; Al = 27;
Pb = 207; H = 1; N = 14; O = 16)
giúp e với ạ
nNO = 2,25/22,4 = 0,1 (mol)
PTHH: R + 4HNO3 -> R(NO3)3 + NO + 2H2O
nR = nR(NO3)3 = nNO = 0,1 (mol)
MR = 2,7/0,1 = 27 (g/mol)
<=> R là nhôm (Al)
Muối thu được: Al(NO3)3
mAl(NO3)3 = 0,1 . 213 = 21,3 (g)
Đúng 2
Bình luận (5)
R+4HNO3->R(NO3)3+NO+2H2O
n NO=\(\dfrac{2,24}{22,4}\)=0,1 mol
=>\(\dfrac{2,7}{M_R}\)=0,1 mol
=>MR=27 g\mol
=>R là Al (nhôm )
->m Al(NO3)3=0,1.213=21,3g
Đúng 2
Bình luận (1)
Đốt cháy hết 2,275 gam một kim loại X trong bình chứa khí Clo. Để nguội bình, thu được 4,76 gam một muối clorua của kim loại X. Xác định tên của kim loại X đem đốt.
\(2X+nCl_2\rightarrow2XCl_n\)
2,275/X -> 4,76/X+35,5n
\(\dfrac{2.275}{X}=\dfrac{4.76}{X+35.5n}\)
=>\(\Leftrightarrow\dfrac{X}{X+35.5n}=\dfrac{2.275}{4.76}=\dfrac{65}{136}\)
=>136X=65X+2307,5n
=>71X=2307,5n
=>X=32,5n
Ta sẽ thấy n=2 phù hợp
=>X=65
=>X là Zn
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn 9,6 gam một kim loại M (chưa rõ hóa trị) trong bình chứa khí clo nguyên chất. Sau khi phản ứng kết thúc, để nguội thì thu được 20,25 gam muối clorua. Kim loại M là A. Fe B. Al C. Cu D. Zn
Đọc tiếp
Đốt cháy hoàn toàn 9,6 gam một kim loại M (chưa rõ hóa trị) trong bình chứa khí clo nguyên chất. Sau khi phản ứng kết thúc, để nguội thì thu được 20,25 gam muối clorua. Kim loại M là
A. Fe
B. Al
C. Cu
D. Zn
Đốt cháy hoàn toàn 4,8 gam một kim loại M hóa trị II trong bình chứa khí clo nguyên chất. Sau khi phản ứng kết thúc, để nguội thì thu được 11,9 gam muối clorua. Kim loại M là
A. Fe.
B. Al.
C. Na.
D. Mg.